Grantová agentura České republiky udělila pro letošní rok celkem 18 grantů Junior Star. Jeden z nich získala Ing. Markéta Hujerová, Ph.D., MBA, z Fakulty textilní Technické univerzity v Liberci (FT TUL ). Uspěla s tématem Next-Generation Antiadhesive Nanofibrous Materials: Fundamental Insights into Their Design and Function, tedy Antiadhezivní nanovlákenné materiály nové generace: Základní poznatky o jejich designu a funkci.
Pětiletý grant Junior Star v celkové výši necelých 14 mil Kč získala liberecká univerzita a Markéta Hujerová za objev léčivé nanonáplasti. Umožní nejen pokračovat v jejím dlouhodobém výzkumu nanomateriálů využitelných v chirurgii, ale tento výzkum ještě zintenzivnit a zvýšit tak šanci na jeho praktické využití. Nanonáplast vyvinutá v Liberci se přiblížila klinickým zkouškám. Znamená revoluci v lékařské péči? S Markétou Hujerovou jsme hovořili nejen o projektu, ale též o výzkumu nanovláken v medicíně obecně.
| Ing. Markéta Hujerová (Klíčová), Ph.D., MBA |
 Je absolventkou Fakulty mechatroniky, informatiky a mezioborových studií TUL (FM) a nyní jako asistentka na FT pracuje na vývoji nanovlákenného a biologicky odbouratelného materiálu pro krytí ran po operacích střev. Spolupracovala s prestižní univerzitou Harvard Medical School. Absolvovala zahraniční postdoc stáži na Institutu Pasteur v Paříži a na National Taiwan University v Tchaj-peji či vědecký pobyt na University of Cambridge. Je absolventkou Fakulty mechatroniky, informatiky a mezioborových studií TUL (FM) a nyní jako asistentka na FT pracuje na vývoji nanovlákenného a biologicky odbouratelného materiálu pro krytí ran po operacích střev. Spolupracovala s prestižní univerzitou Harvard Medical School. Absolvovala zahraniční postdoc stáži na Institutu Pasteur v Paříži a na National Taiwan University v Tchaj-peji či vědecký pobyt na University of Cambridge. Za své vědecké úspěchy si na poli nano připsala řadu ocenění: mezinárodní Cenu publika v rámci Falling Walls Lab (2018), umístění v prestižním žebříčku Forbes 30 po 30 (2021), Cenu ministra školství (2023), Cenu L’Oréal — UNESCO Pro ženy ve vědě (2025) atd. Spin-off Nanoflexion získal 3. místo na Prague.bio Conference 2025, kde soutěžily týmy z Česka i ze zahraničí, a Markéta mohla v létě projekt prezentovat i na EXPO 2025 v japonské Ósace. Pracuje na zlepšení podmínek pro české doktorandy, a to na regionální i národní úrovni. Spolupracuje s Libereckým krajem a pracovala také v neoficiálním poradním orgánu ministryně pro vědu a výzkum Langšádlové a ministra Ženíška. Kromě vědecké práce a vedení projektů si doplnila ekonomické vzdělání na americké University of St. Francis, aby lépe porozuměla světu byznysu a komercializace výzkumu, a získala titul MBA. Studium si financovala z vlastních prostředků. |
Nanonáplast jste vyvinula ještě jako studentka a ve vývoji pokračovala také jako doktorandka. Nyní jste vědecko-pedagogickou pracovnicí na liberecké fakultě textilní. Tímto výzkumem se tedy zabýváte několik let; jak jste daleko?
Začalo to už v průběhu mých studií, kdy jsem zkoumala nanotechnologie a jejich využití v biomedicíně a kdy mě oslovil prof. MUDr. Václav Liška, Ph.D., klinický chirurg a vedoucí Laboratoře nádorové léčby a regenerace tkáně při plzeňském Biomedicínském centru LFP UK.
Hovořili jsme o tom, že operace gastrointestinálního traktu stále představují jistá pooperační rizika, a jeho napadlo, zda bychom pomocí nanotechnologií tato rizika nedokázali omezit. Nabídl mi spolupráci a z jeho popudu jsem toto téma řešila ve své diplomové práci, se kterou jsem pak v roce 2018 vyhrála mezinárodní soutěž Falling Walls Lab pro mladé vědce.
Trochu úsměvné je, že mě inspirovala běžná náplast, když jsem si s ní zalepila krvácející ránu na prstu. Dívala jsem se na to, jak z jedné strany nasákne krev, ale z druhé strany nepřilne k oblečení. Prostě: dvouvrstvé krytí! Uvědomila jsem si, že pro podmínky ve střevech budou nejspíš dvě vrstvy s opačnými vlastnostmi zásadní.
Spolupráce při vývoji nanonáplasti s tak prestižním pracovištěm výrazně zvýšila naše šance dostat se z laboratoře do praxe. A to bylo velmi povzbuzující.
Aktuálně spolupracuji také s biotechnologickým inkubátorem i&i Prague, který vznikl z iniciativy Ústavu organické chemie a biochemie Akademie věd ČR. Výrazným posunem je i dohoda o aplikaci speciální náplasti v klinické praxi.
Naším cílem je převést technologii, která dokáže pacientům skutečně pomoci, do reálné praxe.
Jak vaše nanonáplasti fungují? Můžeme hovořit o bezpečné aplikaci s potenciálem snižovat komplikace?
I přes pokrok v medicíně a vysoký počet operací střev si dosud medicína nenašla spolehlivý způsob, jak zamezit či předejít život ohrožujícím pooperačním komplikacím, jako jsou například srůsty a anastomotický leak [únik obsahu střev do dutiny břišní — pozn. red.]. Naše nanovlákenná náplast je však podle dosavadních výsledků vysoce účinná a má velký potenciál významně snižovat počet komplikací a život ohrožujících stavů po operacích tlustého střeva.
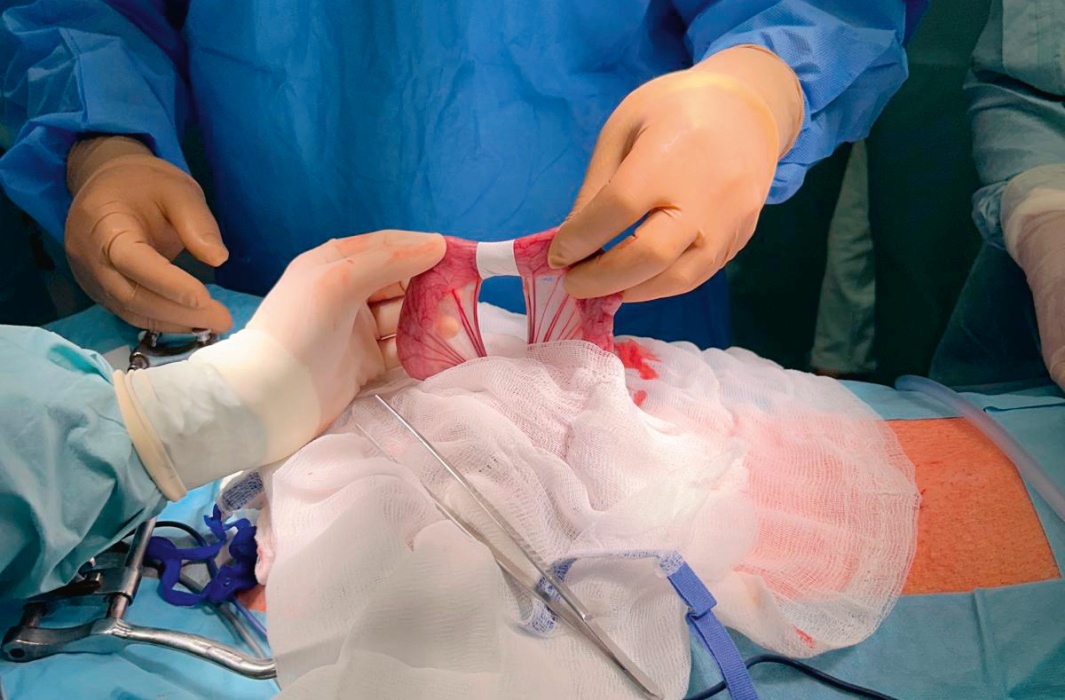
Lidem, kterým při operaci odeberou chirurgové postiženou část střeva, například zasaženou karcinomem, následně standardně sešijí zdravé části orgánu biodegradabilní chirurgickou šicí nití a vytvoří tzv. anastomózu. A právě skrze tuto anastomózu může dojít k prosakování obsahu střeva do dutiny břišní, což bývá příčinou nebezpečné infekce.
Naše „chytré náplasti“ však po sešití střeva anastomózu přikryjí a ochrání ji. Zabraní úniku střevního obsahu, a tím sníží rizika zánětu a septických komplikací. Při operaci se náplast snadno aplikuje, je bezpečná pro tělo a biologicky odbouratelná. Materiál se tedy po určité době v těle sám rozloží, není nutné jej z těla vyjímat.
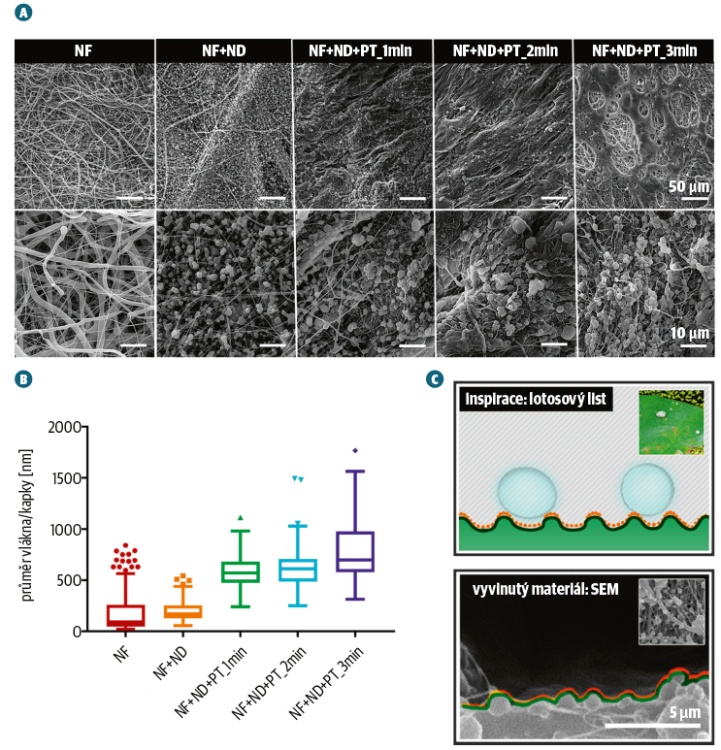
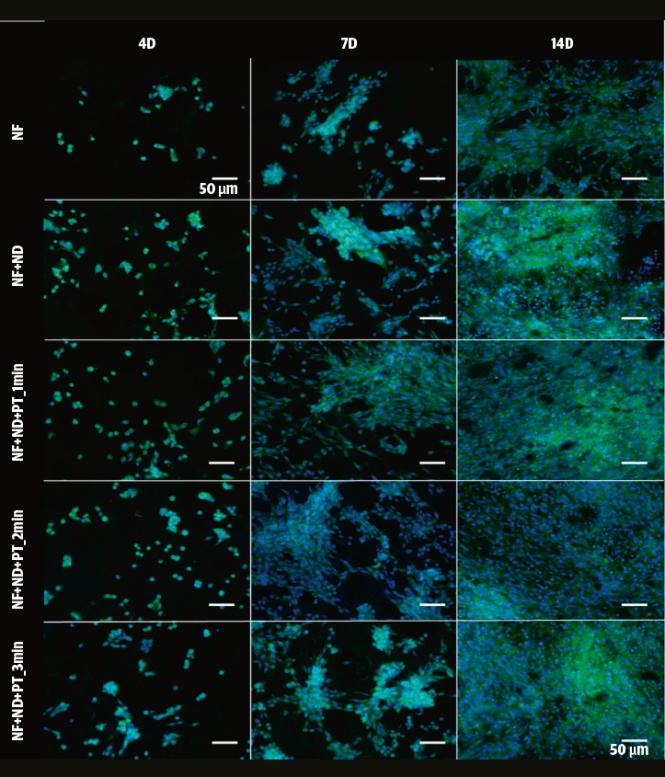
Unikátnost nápadu spočívá v tom, že je náplast tvořena dvěma vrstvami syntetických biodegradabilních polymerů, ze kterých se vyrábějí i chirurgické šicí nitě. My tyto materiály zpracováváme do formy nanovláken a vytváříme vrstvy náplasti podobné mezibuněčné hmotě v lidském těle. Buňkám slouží jako tkáňový nosič (scaffold), na kterém mohou přilnout a růst na něm. Mezi buňkami postupně vznikne nová extracelulární matrix, zatímco náš nanomateriál je tělem absorbován.
Z jedné strany náplasti je adhezní polymer, který velmi dobře přilne k mokré tkáni, druhou stranu tvoří neandhezní polymer s opačnými vlastnostmi. Náplast zpevňuje chirurgickou spojku, slouží jako mechanická podpora tkáně a zabrání tvorbě srůstů. Náplasti lze navíc „doplnit“ léčivými látkami, které se postupně uvolňují přímo do místa zákroku, urychlí hojení a zabrání infekci.
Zatím tyto látky nebudu konkretizovat, protože připravujeme patentovou přihlášku a je to naše obchodní tajemství. Ale mohu konstatovat, že podobný materiál na trhu zatím chybí. Osobně jsem přesvědčena, že díky spolupráci všech zainteresovaných týmů se transfer podaří a že do několika let bude naše nanonáplast pomáhat pacientům v nemocnicích.
Transfer a komercionalizace vašeho výzkumu, to byl důvod, proč zakládáte univerzitní spin-off Nanoflexion. Jaký je cíl?
K záměru založit spin-off Nanoflexion na Fakultě textilní TUL jsem přistoupila z praktického důvodu: když jsme vážně začali uvažovat o tom, že bychom měli výsledky našeho výzkumu více transferovat do praxe a do reálného byznysu. Uvědomila jsem si, že k tomu, abychom se posunuli dál a nanonáplast nezůstala v laboratořích jen jako zajímavý nápad, musíme být v kontaktu s aktuálním průmyslem. Že musíme řešit i technické záležitosti, regulatorní procesy a také spolupráci se strategickými partnery, vstup investora i otázky inovace atd.
Před tím jsem byla „jenom“ vědkyně, která vyvinula a v laboratoři ověřila funkční nanonáplast a jež vyvíjí a zkoumá něco, z čeho i přes pozitivní ohlas ve vědeckém světě nemusí vzniknout reálně nic. Ale já chtěla, aby se náš výzkum dostal na chirurgické sály.
V určité fázi mi prostě došlo, že „dělat čistou vědu“ nestačí, a že pokud chceme naši náplast skutečně dostat až k lidským pacientům, musíme se aktivně zabývat komercializací a transferem technologií. K tomu bylo potřeba založit spin-off a odpoutat se od čisté vědy.
Diskutovali jsme o tom ze začátku hlavně na půdě biotech inkubátoru i&i Prague, který prozíravě investuje do vědeckých týmů. Myslím, že je tam zřejmá inspirace mimořádně úspěšným transferem objevu Antonína Holého, jehož lék Viread díky léčivé látce tenofovir umožňuje snížit hladinu HIV. V srpnu 2025 jsme s biotechnologickým inkubátorem i&i Prague uzavřeli inkubační smlouvu a jsme nyní jedním z jeho inkubovaných spin-offů. Důležitým bodem smluv je, že naše výsledky vědy a výzkumu budou transferovány do reálné praxe.
Díky podpoře i&i Prague získal náš projekt nejen finanční zázemí, ale také mentoring a strategické vedení. Spin-off Nanoflexion ještě spoluvlastní Technická univerzita v Liberci a Lékařská fakulta UK v Plzni. Společně se v něm zaměřujeme na prevenci pooperačních komplikací v gastrointestinální chirurgii právě s pomocí těchto speciálních nanovlákenných náplastí a řešíme i další kroky technologického transferu.
Dobrou zprávou je, že jsme získali pozornost i na mezinárodní úrovni, když jsme loni Nanoflexion prezentovali na světové výstavě Expo v Ósace.
Z našeho rozhovoru vyplynulo, že vámi vyvinutá nanonáplast se přiblížila klinickým zkouškám. Znamená to revoluci v lékařské péči?
Od roku 2018, kdy jsem se tématu začala věnovat systematicky, jsme ušli velký kus cesty. Získaná data potvrzují, že má smysl se této problematice věnovat dlouhodobě, a současně máme velmi slibné výsledky na preklinických modelových systémech.
Ve spolupráci s Biomedicínským centrem Lékařské fakulty Univerzity Karlovy v Plzni jsme náplasti testovali na velkém zvířecím modelu — na prasatech. To je velká výhoda, protože často není možné testovat na zvířatech, eventuálně jenom na malém zvířecím modelu, například na potkanech. Z prasat dostáváme zajímavá data a podařilo se nám vylepšit náplast tak, že skutečně zabraňuje úniku obsahu střev do dutiny břišní (anastomotickému leaku). Jsme tedy velmi blízko klinické praxi a vytvoření prvních vzorků pro testování na pacientech.
Dostat naši náplast na trh a k pacientům je v tuto chvíli moje největší motivace. Samozřejmě si na dosažení tohoto cíle budeme muset ještě počkat.
Vývoj zdaleka nekončí, ale cesta ke klinické praxi je otevřena. Co to znamená? Budou se už nanonáplasti testovat na lidech? Co tomu předcházelo?
Dá se říci, že momentálně pracujeme paralelně na dvou frontách: vědecký výzkum v laboratoři dále pokračuje a zároveň intenzivně rozvíjíme proces komercializace, aby se naše technologie mohla co nejrychleji posunout směrem k reálnému využití v chirurgické praxi.
Ve výzkumu v laboratořích nám významně pomůže již zmiňovaný pětiletý grant Junior Star, s jehož podporou se mi podařilo vytvořit novou stabilní vědeckou skupinu i podmínky pro další výzkum v oblasti nanotechnologií v biomedicíně. Projekt financovaný z grantu GA ČR a o jehož udělení rozhodli zahraniční oponenti, spadá do oblasti základního výzkumu. Základní výzkum znamená, že předmětem výzkumu není funkční náplast jako finální produkt a její uplatnění v praxi. Je však dost oblastí pro práci v laboratoři, na které se v něm chceme zaměřit.
Intenzivně se například zabýváme možnostmi inkorporace různých léčiv do náplasti.
Cílem je také experimentální objasnění zásadní otázky, která dosud nemá ve vědeckém světě jednoznačnou odpověď: Jaké povrchové vlastnosti musí mít antiadhesivní materiál, aby účinně bránil vzniku pooperačních srůstů? Tato funkce totiž stále není dostatečně vědecky podložena.
Některé studie uvádějí, že nejlepší antiadhesivní efekt mají extrémně hydrofilní (smáčivé) povrchy, jiné tvrdí, že klíčem jsou povrchy vysoce hydrofobní, tedy materiály odolávající pronikání vody a vlhkosti, někdo preferuje lubrikační vlákna. Dodnes tedy nemáme jasně definováno, jaký typ povrchu skutečně brání tvorbě pooperačních srůstů ani jaký materiál je vhodný pro jiné medicínské aplikace. To je neprobádané téma a cílem našeho projektu základního výzkumu je vědecky odpovědět na nezodpovězené otázky a experimentálně objasnit a detailně popsat, jaké má mít materiál vlastnosti a jaké faktory tyto vlastnosti ovlivňují.
Zaměříme se na vlastnosti polymerů z hlediska povrchu nebo kontaktu s buněčnými kulturami, budeme řešit adhezi, a to i na kadaverózních (mrtvých, z těla vyjmutých) tkáních, abychom nemuseli používat drahé zvířecí modely. Ve hře je také materiál, který má být z jedné strany přilnavý (adhesivní) ke střevní tkáni, kde pomáhá k hojení rány, ale z druhé strany musí zůstat nelepivý — antiadhesivní — tak, aby rána nesrůstala s okolní tkání. Pak by se nemuselo jednat o dvouvrstvé krytí.
Díky projektu můžeme intenzivně pracovat v laboratořích a psát impaktované články, samozřejmě s vizí, že naše závěry základního výzkumu přejdou do výzkumu aplikačního.
O nanovláknech mluvíte jako o materiálu budoucnosti, jaké jsou výhody nanovláken v oblasti medicíny?
Jsem přesvědčena, že se jedná o materiál, který dokáže změnit svět. Populárně se uvádí, že nanovlákna jsou až 10 000× tenčí než lidský vlas. Svojí strukturou napodobují mezibuněčnou hmotu, čímž podporují růst nových buněk a přirozené hojení bez jizev. Splétají se v jemné pavučinky, a vznikají tak speciální textilie, které poskytují lešení (scaffoldy) pro růst buněk a jsou ideální pro podporu obnovy tkání. Na tomto scaffoldu je možné pěstovat třeba i umělé orgány pro testování nových léků.
A právě této vlastnosti jsem využila při vývoji nanonáplasti. Nanovlákna mají obrovský potenciál, protože naše tělo je na ně vlastně zvyklé. Naše mezibuněčná hmota, která je všude mezi našimi buňkami, je vlastně změť mikro- a nanovláken. Tím pádem naše tělo nanovlákna velmi dobře přijímá. Když se vyskytne nějaké komplikované poranění, třeba popálenina, nanovlákna mohou poskytnout lešení pro výstavbu nových buněk. Rány se rychleji zahojí, lépe a rychleji srostou, ideálně bez jizev.
Na stejném principu by mohla do budoucna fungovat i případná kultivace částí, nebo — ideálně — celých orgánů. K tomu ale bude určitě potřeba kombinace více technologií. Na to samotná nanovlákna nejspíše stačit nebudou, i když budou mít určitě významnou funkci. Tady jsme tedy zatím ve světě přání a fantazie, ale cílem je, abychom mohli v laboratoři vypěstovat lešení pro jednotlivé orgány, třeba srdce, které následně budeme moci dát pacientovi, a on nebude muset čekat na vhodného dárce. Zatím však nikdo ledvinu, srdce ani jiný orgán v laboratoři nevypěstoval. Nestojí to samozřejmě jen na nanomateriálech, největší problém je komplexita orgánů. Nanomateriály tam ovšem budou hrát obrovskou roli.
Zdůrazňujete, že pro vývoj nových materiálů jsou důležití partneři z průmyslu. Jaká je podpora průmyslu pro výzkum v této oblasti?
Dnes se řada firem zabývá aplikacemi pro biomedicínu. Vědecké týmy spolupracují s lékaři apod. V tisku například proběhla prezentace superpřesné nanotiskárny IQnano3D, na které lze vyrábět nanostruktury s přísně řízenou strukturou. Využívá takzvanou dvoufotonovou litografii. Díky ní je možné připravit malé implantáty s vysokou přesností, na míru danému pacientovi. To je velký posun kupředu. Nová technologie má při vysokém rozlišení díky využití femtosekundového laseru výrazně vysokou přesnost a vysoký stupeň rozlišení. V konkrétním bodě, kde zasvítí, se ten materiál soldifikuje, tedy změní skupenství z kapalného na pevné. Takto se postupně, odspodu vrstva po vrstvě vytiskne celý, velmi malý objekt — třeba i mikroimplantát v nějakém malém objektu.
Vývoj jde rychle dopředu a myslím, že v dohledné době mohou být vyvinuty tiskárny dalších generací, které přiblíží představu, že je možné tisknou implantáty s vysokou přesností a na míru danému pacientovi, nebo by se to mohlo uplatnit i při poranění nervových vláken, kdy malé nosiče — scaffoldy — usnadní růst neuronů.
Tiskárnou lze do diagnostických čipů dotisknout také menší funkční struktury, ale i to je otázkou dalšího výzkumu.
Hovoří se také o orgánech na čipu. Dočkáme se i umělých orgánů pro transplantaci?
Vývoj umělých orgánů pro transplantaci nebo alespoň částí jednotlivých tkání je podle mne slibnou oblastí. Buňky lidského těla na nanovlákna dobře reagují a porůstají je. Věřím, že jednou dokážeme alespoň některé orgány vyrobit v laboratoři, a zkrátíme tak sáhodlouhý seznam čekatelů na vhodného dárce, který se třeba ani nikdy nenajde.
Co se týče orgánů na čipu, to je něco zcela jiného. Tímto výzkumem se vědecké týmy leckde zabývají, včetně nás v Liberci. Na naší univerzitě běží projekt podpořený TAČR — Národním centrem kompetence. Řeším v něm se svými kolegy z univerzity a z firmy IQS nano projektový balíček zaměřený na mikrofluidní systémy, které umožňují manipulaci s malými objemy tekutin. Ty jsou využitelné právě pro výzkum orgánů na čipu. Což ale neznamená, že se vypěstuje orgán, třeba umělá ledvina, a transportuje se do těla.
Jde vlastně o předaplikační způsob detekce kvality léčiva mimo tělo. Laicky řečeno: vytvoří se imitace, nebo chcete-li malá napodobenina našich jednotlivých orgánů, se kterými lze snadno pracovat v laboratoři a s jejichž pomocí lze simulovat fungování celých orgánů. Do nich se aplikuje zkoumaná látka a sleduje se reakce.
Orgány na čipu jsou vlastně polymerové obdélníky o velikosti flashdisku. Jsou brázděné propojenými mikrokanálky a uprostřed je malinká část vystlaná živými lidskými tkáněmi imitujícími konkrétní orgán. Může to být ledvina, játra, střevo nebo i kůže, a pokud by se podařilo vyvinout všechny napodobeniny lidských orgánů a napojit je na sebe, dostali bychom vlastně lidské tělo na čipu jako celek.
Jedná se o zařízení, která umožňují otestovat přímo na lidských tkáních systémovou odezvu orgánu třeba na léčivo, aniž by se jakkoliv ohrozil člověk. Tento výzkum má také velký etický dopad, protože by se výrazně omezily pokusy na zvířatech. Na nich by se otestovala pouze poslední fáze pokusů zaměřených na koncentraci léčivých látek. Přibližují nás k účinnější personalizované medicíně, tedy k aplikacím léčivých látek podle individuálních problémů konkrétního pacienta.
Na takovém výzkumu jste pracovala také na Harvardu. Jak vás studium na této prestižní univerzitě ovlivnilo?
Profesor Donald E. Ingber, u kterého jsem tam byla na stáži, se snažil tímto způsobem v laboratoři napodobit jednotlivé orgány — jejich strukturu a funkci. Imitoval na čipu ledvinu, plíce i další orgány. Už dokázal na čipech napodobit třeba funkci plic. Na čip se nasadí plicní buňky, v čipu proudí krev, vzduch a buňky mají stejné podmínky, jako mají přirozeně buňky v našem těle. Když pak přišla pandemie covidu- 19, profesor velmi rychle dokázal v laboratoři nakazit tyto umělé plíce třeba covidem nebo tuberkulózou a díval se, jak reagují na různé experimentální léky.
A toho jsem se přímo účastnila. Americký systém studia se totiž od našeho dost liší. Tím, že vás neustále motivuje k tomu, abyste se zapojili do vědecké práce, měli jste ambice a snažili se je naplnit. Mladí vědci jsou systematicky vedeni k vlastní aktivitě a k tomu, aby jejich výzkum měl nějaký reálný dopad. Profesor předloží studentovi problém a řekne: „Ty ho budeš řešit a já ti s tím eventuálně pomůžu.“ Je tam méně dlouhých (a povinných) přednášek, při kterých student jen sedí a pasivně si něco zapisuje. Proto se tam zakládá daleko více spin-offů.
Zatímco tam je to běžná záležitost, u nás to je spíš výjimka. I na naší univerzitě máme jen dva, z toho je jeden ten náš Nanoflexion.
Mohu potvrdit, že na Harvardu studenti a mladí vědci pracují na vědě mnohem tvrději a mají realističtější a konkrétnější cíle, protože jsou si vědomi, že to bude jejich budoucí obživa, jejich byznys. Studovat jen kvůli diplomu se tam moc nenosí. Budu se snažit, aby se tato „studijní atmosféra“ přenesla i k nám.
Na změně studijního přístupu se asi podílet můžete, když vedete studenty, kteří se na TUL podílí na tkáňovém inženýrství, a veřejně upozorňujete na nedostatečné podmínky pro jejich vědeckou práci.
Chci upozorňovat na to, že podmínky pro mladé vědce a vědkyně jsou obtížné a víceméně brání tomu, aby se obor nanotechnologií a nanomateriálů u nás rozvíjel a abychom nezaostali za světem.
Mladí vědci, studenti doktorského studia ve věku 25—30 let jsou výraznou součástí české vědy. Zkoumají v laboratořích, učí se psát projekty, odvádějí obrovský podíl na psaní vědeckých publikací, prezentují v angličtině v zahraničí a snaží se vytipovat nové směry. Jejich finanční podmínky jsou ale nedostatečné a studenti si pak musí hledat druhou práci, což způsobuje pracovní zahlcení a menší soustředění na vědu a ještě hůře: na budování osobních vztahů.
Je vlastně obdivuhodné, že se mladý inženýr nebo inženýrka rozhodnou jít na doktorské studium, když tam dostanou několikanásobně nižší plat, než by dostali v jakékoliv firmě. Je třeba zaměřit se na to, že doktorandi jsou nezbytným článkem celého výzkumu. Pokud se chtějí věnovat vědě a mít i rodinu, je to pro ně problematické a řadu studentů to možná i od vědecké práce odradí, vždyť například doktorandka nemá ani nárok na mateřskou a nedosáhne na hypotéku.
Nutná je také správná podpora projektů pro mladé studenty, více juniorských grantových projektů, to vše pomůže vědu podpořit. Dlouhodobé financování je pro systematický výzkum naprosto klíčové. Nám například získaný grant pomohl v tom, že mohu přijmout nové doktorandy a vybudovat vlastní tým schopných a zdravě ambiciózních kolegů. A kromě vědecké práce se s celým týmem budeme i nadále snažit poukazovat na nedostatky české vědy a motivovat mladé lidi, aby se aktivněji zapojovali nejen do základního, ale i aplikačního výzkumu.